前沿 | 复旦大学发文揭示癌症转移最新分子机制和预防靶点-pg电子官方
近日,复旦大学研究团队在期刊《cancer letters》上在线发表题为“circube3a(2,3,4,5) promotes adenylate-uridylate-rich binding factor 1 nuclear translocation to suppress prostate cancer metastasis”的研究论文,本研究将circube3a(2,3,4,5)表征为一种功能性circrna,并将其作为预防前列腺癌转移的极具前景的靶点。

研究背景
前列腺癌(pca)是男性中主要的恶性肿瘤,其每年的发病率持续上升,2023年占据全球男性癌症新发病例的29%。手术干预和放射治疗仍然是局部pca的有效治疗方式。然而,在转移性前列腺癌治疗中,迫切需要改进的治疗方案。因此,探索调控pca转移的分子机制并开发有效干预措施至关重要。
环状rna(circrnas)是一类独特的共价闭合非编码rna亚群,具有独特的结构特征、出色的稳定性、高保守性和丰富的表达。已经确定,侧翼内含子互补序列是导致circrna形成的反向剪接的重要贡献者。在功能上,circrnas可以通过作为蛋白质复合物的支架或与rna结合蛋白(rbps)相互作用来调节基因表达,影响基因的表达,包括它们的亲本基因。它们还可以作为micrornas(mirnas)的分子海绵,并展示出编码肽的能力,例如circccdc7(15,16,17,18,19)和circ-fbxw7。越来越多证据表明,circrnas在调控各种癌症中发挥着关键作用,使它们有望成为临床生物标志物和可行的治疗干预靶点。
研究发现
这项研究利用体外筛选细胞模型和高通量circrna测序系统,鉴定了一个与前列腺癌(pca)相关的circrna(circbase id: hsa_circ_0000586)。由于它来源于泛素蛋白连接酶e3a(ube3a)基因的四个外显子(外显子2、3、4和5),研究人员按照最新的命名指南将其命名为circube3a(2,3,4,5)。发现circube3a(2,3,4,5)在pca组织中下调,并与肿瘤恶性相关。它通过与auf1相互作用并促进其向细胞核的易位来抑制pca的转移。因此,auf1在细胞质中的缺乏导致mthfd2 mrna稳定性降低,导致波形蛋白表达下调。两对短倒置重复序列 (tsir) 被鉴定为协同增强 circube3a(2,3,4,5) 的形成。研究发现揭示了circrna在转移中新的调控作用,并确定了治疗pca转移的新分子机制。
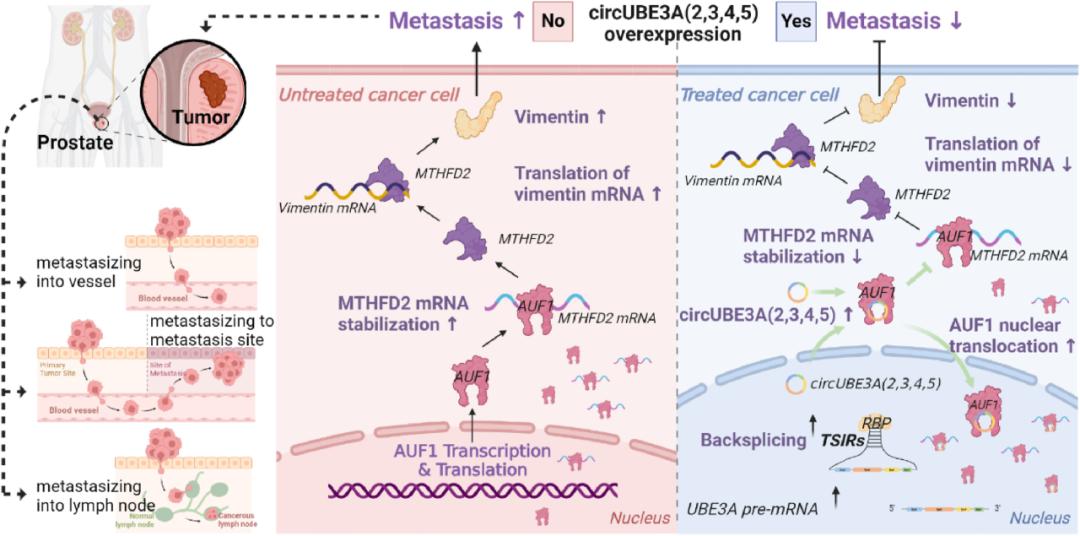
研究结论
综上所述,本研究将circube3a(2,3,4,5)表征为一种功能性circrna,并将其作为预防前列腺癌转移的极具前景的靶点。(来源:)
参考资料:
https://www.sciencedirect.com/science/article/pii/s0304383524001368